पीएच पर निर्भर करता है। हाइड्रोजन सूचकांक (पीएच कारक)
इस लेख में, हम शराब की अम्लता क्या है और यह कैसे निर्धारित किया जाता है, के सवालों का जवाब देते हैं। पीएच क्या है और उपभोक्ता को यह क्यों जानना चाहिए। शराब की डिग्री क्या है।
शराब की डिग्री
इनमें से एक संक्षिप्तीकरण बहुत सरल है - ABV का अर्थ है अंग्रेजी "अल्कोहल बाय वॉल्यूम", अर्थात। तरल मात्रा में अल्कोहल सामग्री (हमारे मामले में, इथेनॉल)। आमतौर पर प्रतिशत के रूप में मापा जाता है। और बोलचाल की भाषा में इसे डिग्री कहते हैं। उदाहरण के लिए, चालीस डिग्री वोदका की अभिव्यक्ति का मतलब है कि प्रस्तावित समाधान में मात्रा के हिसाब से 40% - चालीस प्रतिशत अल्कोहल है।
वॉल्यूम प्रतिशत या डिग्री को 20 डिग्री सेल्सियस के तापमान पर 100 मिलीलीटर की मात्रा में "शुद्ध" इथेनॉल के मिलीलीटर में मापा जाता है।
संक्षेप में, यह स्पष्ट है कि यदि बोतल ABV 5.5% इंगित करती है, उदाहरण के लिए, कुछ Moscato d'Asti वाइन पर, तो इस कम-कार्बोनेटेड और कम-अल्कोहल वाइन को बिना किसी डर के पूरी शाम हल्के से घूंट-घूंट कर पीया जा सकता है। अगले दिन हैंगओवर। जैसा कि वे कहते हैं, केफिर में अधिक शराब है!
वैसे, यही कारण है कि मोसेटो डी एस्टी और एक अन्य इतालवी स्पार्कलिंग वाइन, प्रोसेको, हॉलीवुड पार्टियों में इतनी लोकप्रिय हैं। हर कोई पूरी शाम हाथ में गिलास लेकर चलता है, लेकिन शराबी नहीं होते। और आप खुद घर चला सकते हैं। हालांकि खबरों को देखते हुए, इन पार्टियों के प्रतिभागियों को वास्तव में बाद के विचार की परवाह नहीं है।
थोड़ा सा सिद्धांत - क्या है पीएच
सहज स्तर पर, हम सभी मोटे तौर पर समझते हैं कि अम्लता क्या है। "अम्लता" की डिग्री, इसलिए बोलने के लिए। रसायन विज्ञान में, यह शब्द अम्लता, अव्यक्त है। एसिडिटास, इंजी। अम्लता - समाधान और तरल पदार्थ में हाइड्रोजन आयनों की गतिविधि की विशेषता को दर्शाता है।
सच्ची (सक्रिय) और कुल (टिट्रेटेबल) अम्लता हैं। जलीय घोलों में, अकार्बनिक पदार्थ, अर्थात। लवण, अम्ल और क्षार (भंग) उनके घटक आयनों में अलग हो जाते हैं।
इसी समय, सकारात्मक रूप से आवेशित हाइड्रोजन आयन एच +अम्लीय गुणों के वाहक और ऋणावेशित आयन होते हैं ओह-(उन्हें हाइड्रॉक्सिल्स भी कहा जाता है) - क्षारीय गुणों के वाहक।
सौ साल पहले, रसायनज्ञों ने एक विशेष हाइड्रोजन सूचकांक पेश किया, जिसे आमतौर पर प्रतीकों द्वारा दर्शाया जाता है पीएच.
थोड़ा गणित
गैर-न्यूडिस्ट (सी) और गैर-गणितज्ञ (सी) इस पैराग्राफ को छोड़ सकते हैं। और बाकी के लिए, हम आपको सूचित करेंगे कि जलीय घोलों के लिए, संतुलन समीकरण लागू होता है - H + और OH- आयनों की गतिविधि का गुणनफल स्थिर होता है। तथाकथित सामान्य परिस्थितियों में, यानी। 22 डिग्री सेल्सियस और सामान्य दबाव के पानी के तापमान पर, यह 10 से घटाकर 14वीं शक्ति के बराबर है।
1909 में डेनिश बायोकेमिस्ट सोरेनसेन ने पीएच मान पेश किया, जो परिभाषा के अनुसार हाइड्रोजन आयनों की गतिविधि के दशमलव लघुगणक के बराबर है, जिसे माइनस के साथ लिया गया है:
पीएच= - एलजी (एच + गतिविधि)
एक तटस्थ माध्यम में, जैसा कि हमने अभी कहा, आयनों की गतिविधियाँ समान होती हैं, अर्थात। H+ गतिविधि और OH- गतिविधि का गुणनफल H+ गतिविधि के वर्ग के बराबर होता है। और यह 10 के माइनस 14वें घात के बराबर है।
तो, 14 को 2 से विभाजित करने के बाद, नकारात्मक दशमलव लघुगणक 7 के बराबर होगा। इसका मतलब है कि (22 डिग्री सेल्सियस के तापमान पर) शुद्ध पानी की अम्लता, यानी तटस्थ अम्लता, सात इकाइयों के बराबर है: पीएच= 7.
समाधान और तरल पदार्थ अम्लीय माने जाते हैं यदि वे पीएच 7 से कम, और क्षारीय, यदि अधिक हो।
आमतौर पर, शराब सहित खाद्य उत्पाद अम्लीय होते हैं। क्षारीय प्रतिक्रियाएं रासायनिक आटा रिसाव एजेंट (सोडा, अमोनियम कार्बोनेट) और उनके उपयोग से तैयार उत्पाद, जैसे कुकीज़ और जिंजरब्रेड हैं।
तीन प्रकार की अम्लता
चलो अपराध बोध पर वापस आते हैं। शब्द "अम्लता" वाइन के विश्लेषण, विवरण और उत्पादन में सबसे अधिक उपयोग में से एक है। वास्तव में, अम्लता वाइन रसायन और स्वाद की सबसे महत्वपूर्ण विशेषताओं में से एक है। वाइनमेकिंग में तीन प्रकार की अम्लता होती है:
- कुल या अनुमापित
- सक्रिय या सत्य - यह गतिविधि का [हाइड्रोजन] सूचक है पीएच
- वाष्पशील अम्लता
अनुमाप्य अम्लता
टिट्रेटेबल या कुल अम्लता रस या वाइन में सभी मुक्त अम्लों और उनके अम्ल लवणों की समग्रता को निर्धारित करती है।
इसका मूल्य इन अम्लों को बेअसर करने के लिए आवश्यक क्षार (उदाहरण के लिए, कास्टिक सोडा या पोटेशियम) की मात्रा से निर्धारित होता है। अर्थात्, क्षार की वह मात्रा जिसे शराब में मिलाया जाना चाहिए ताकि इससे बिल्कुल तटस्थ घोल प्राप्त किया जा सके (pH = 7.0)।
कुल अम्लता ग्राम प्रति लीटर में मापा जाता है।
सक्रिय अम्लता
सक्रिय या सच्ची अम्लता पीएच . गणितीय रूप से, यह हाइड्रोजन आयनों की सांद्रता का ऋणात्मक लघुगणक है, जैसा कि ऊपर बताया गया है। तकनीकी रूप से, यह शराब की अम्लता का सबसे सटीक उपाय है।
यह शराब में निहित सबसे मजबूत एसिड की मात्रा पर निर्भर करता है। मजबूत अम्ल वे होते हैं जिनका पृथक्करण स्थिरांक (Kd) [एसिड] सबसे अधिक होता है।
"ताकत" द्वारा आदेशित ठेठ एसिड का एक उदाहरण, जो पृथक्करण स्थिरांक (एसिड की डिग्री) के अवरोही क्रम में है:
- लेमन सीडी = 8.4 10-4
- एम्बर सीडी = 7.4 10-4
- सेब सीडी = 3.95 10-4
- डेयरी केडी = 1.4 10-4
मान से पीएच प्राथमिक और माध्यमिक किण्वन उत्पादों के मात्रात्मक अनुपात पर निर्भर करता है, शराब की ऑक्सीकरण, क्रिस्टलीय और जैविक मैलापन की प्रवृत्ति, दोषों के प्रति संवेदनशीलता और शराब रोगों के प्रतिरोध पर निर्भर करता है।
उदाहरण
लघुगणक संबंध की एक सरल व्याख्या। के साथ समाधान पीएच= 3 एक विलयन की तुलना में दस गुना अधिक अम्लीय है पीएच= 4. या, अधिक व्यावहारिक उदाहरण के लिए, वाइन के साथ पीएच= 3.2 25% अधिक अम्लीय शराब के साथ पीएच= 3.3.
यदि वाइन की अम्लता को सही करना आवश्यक है, तो वाइन निर्माता 1.9 g/l लैक्टिक एसिड और 2.27 g/l टार्टरिक (डाइऑक्सिसुसिनिक या टार्टरिक) एसिड का मिश्रण मिलाते हैं। इससे इसे कम करना संभव हो जाता है पीएचलगभग 0.1 (रेंज 3 से 4)।
और अगर, उदाहरण के लिए, शराब पीएच = 3.7 के साथ निकली और वाइनमेकर इसे पीएच = 3.5 पर लाना चाहता है, तो वह इस "खुराक" को दोगुना कर देगा।
मूल्यपीएचकुछ उत्पादों के लिए
नीचे दी गई तालिका कुछ सामान्य खाद्य पदार्थों और विभिन्न तापमानों पर शुद्ध पानी के अम्लता मूल्यों को दर्शाती है:
| उत्पाद | पेट की गैस, पीएच |
| नींबू का रस | 2,1 |
| शराब, लगभग। | 3,5 |
| टमाटर का रस | 4,1 |
| संतरे का रस | 4,2 |
| ब्लैक कॉफ़ी | 5,0 |
| 100 डिग्री सेल्सियस पर शुद्ध पानी | 6,13 |
| 50 डिग्री सेल्सियस पर शुद्ध पानी | 6,63 |
| ताजा दूध | 6,68 |
| 22 डिग्री सेल्सियस पर शुद्ध पानी | 7,0 |
| 0 डिग्री सेल्सियस पर शुद्ध पानी | 7,48 |
वाष्पशील अम्लता
वाष्पशील अम्लता, या संक्षेप में वीए, शराब में एसिड का वह हिस्सा है जिसे नाक से पता लगाया जा सकता है।
उन अम्लों के विपरीत जो स्वाद के लिए सुपाच्य होते हैं (जैसा कि हमने ऊपर बात की थी)।
वाष्पशील अम्लता, या दूसरे शब्दों में, शराब का खट्टा होना, सबसे आम दोषों में से एक है। इसके मुख्य अपराधी एसिटिक एसिड (सिरके की तरह महक) और इसके एस्टर, एथिल एसीटेट (नेल पॉलिश की तरह महक) हैं।
वाष्पशील अम्लता के लिए जिम्मेदार जीवाणु कम अम्लता और उच्च चीनी सामग्री की स्थितियों में पनपते हैं। कम सांद्रता में, वाष्पशील अम्लता शराब को चटपटापन देती है। और जब दहलीज पार हो जाती है, सिरका-लाह घटक उपयोगी अरोमा को रोकता है और शराब के स्वाद को खराब करता है।
हाइड्रोजन सूचकांक - पीएच - एक समाधान में हाइड्रोजन आयनों की गतिविधि का एक उपाय है (पतला समाधान के मामले में यह एकाग्रता को दर्शाता है), इसकी अम्लता को मात्रात्मक रूप से व्यक्त करते हुए, एक नकारात्मक (विपरीत चिह्न के साथ लिया गया) के दशमलव लघुगणक के रूप में गणना की जाती है। हाइड्रोजन आयनों की गतिविधि, मोल प्रति लीटर में व्यक्त की जाती है।
पीएच = - एलजी
यह अवधारणा 1909 में डेनिश रसायनज्ञ सोरेनसेन द्वारा पेश की गई थी। संकेतक को पीएच कहा जाता है, लैटिन शब्द पोटेंशिया हाइड्रोजनी के पहले अक्षरों के बाद - हाइड्रोजन की ताकत, या पोंडस हाइड्रोजनी - हाइड्रोजन का वजन।
पारस्परिक पीएच मान कुछ कम व्यापक हो गया है - समाधान की मूलभूतता का एक संकेतक, पीओएच, ओएच आयनों के समाधान में एकाग्रता के नकारात्मक दशमलव लघुगणक के बराबर:
पीओएच = - एलजी
25 ° C पर शुद्ध पानी में, हाइड्रोजन आयनों () और हाइड्रॉक्साइड आयनों () की सांद्रता समान होती है और 10 -7 mol / l की मात्रा होती है, यह सीधे पानी के ऑटोप्रोटोलिसिस निरंतर K w से होता है, जिसे अन्यथा आयन कहा जाता है पानी का उत्पाद:
के डब्ल्यू \u003d \u003d 10 -14 [मोल 2 / एल 2] (25 डिग्री सेल्सियस पर)
पीएच + पीओएच = 14
जब किसी विलयन में दोनों प्रकार के आयनों की सांद्रता समान होती है, तो विलयन को उदासीन कहा जाता है। जब एक एसिड को पानी में जोड़ा जाता है, तो हाइड्रोजन आयनों की सांद्रता बढ़ जाती है, और हाइड्रॉक्साइड आयनों की सांद्रता तदनुसार कम हो जाती है, जब एक आधार जोड़ा जाता है, इसके विपरीत, हाइड्रॉक्साइड आयनों की सामग्री बढ़ जाती है, और हाइड्रोजन आयनों की एकाग्रता कम हो जाती है। कब > वे कहते हैं कि समाधान अम्लीय है, और कब > - क्षारीय।
पीएच निर्धारण
समाधानों के पीएच मान को निर्धारित करने के लिए कई विधियों का व्यापक रूप से उपयोग किया जाता है।
1) पीएच मान संकेतकों के साथ अनुमानित किया जा सकता है, पीएच मीटर के साथ सटीक रूप से मापा जाता है, या एसिड-बेस अनुमापन करके विश्लेषणात्मक रूप से निर्धारित किया जाता है।
हाइड्रोजन आयनों की सांद्रता के मोटे अनुमान के लिए, एसिड-बेस संकेतकों का व्यापक रूप से उपयोग किया जाता है - कार्बनिक डाई पदार्थ, जिसका रंग माध्यम के पीएच पर निर्भर करता है। सबसे प्रसिद्ध संकेतकों में लिटमस, फिनोलफथेलिन, मिथाइल ऑरेंज (मिथाइल ऑरेंज) और अन्य शामिल हैं। संकेतक दो अलग-अलग रंगीन रूपों में मौजूद हो सकते हैं, या तो अम्लीय या बुनियादी। प्रत्येक संकेतक का रंग परिवर्तन इसकी अम्लता सीमा में होता है, आमतौर पर 1-2 इकाइयाँ (तालिका 1, पाठ 2 देखें)।
पीएच माप की कार्य सीमा का विस्तार करने के लिए, तथाकथित सार्वभौमिक संकेतक का उपयोग किया जाता है, जो कई संकेतकों का मिश्रण है। एक अम्लीय से क्षारीय क्षेत्र में जाने पर सार्वभौमिक संकेतक लगातार लाल से पीले, हरे, नीले से बैंगनी रंग में बदलता है। सांकेतिक विधि द्वारा pH का निर्धारण मेघमय या रंगीन विलयनों के लिए कठिन होता है।
2) विश्लेषणात्मक वॉल्यूमेट्रिक विधि - एसिड-बेस अनुमापन - भी समाधानों की कुल अम्लता का निर्धारण करने के लिए सटीक परिणाम देता है। परीक्षण विलयन में ज्ञात सान्द्रता (टाइट्रेट) का विलयन बूंद-बूंद करके डाला जाता है। जब वे मिश्रित होते हैं, तो एक रासायनिक प्रतिक्रिया होती है। तुल्यता बिंदु - वह क्षण जब टाइट्रेंट पूरी तरह से प्रतिक्रिया को पूरा करने के लिए पर्याप्त होता है - एक संकेतक का उपयोग करके तय किया जाता है। इसके अलावा, जोड़ा टाइट्रेंट समाधान की एकाग्रता और मात्रा को जानने के बाद, समाधान की कुल अम्लता की गणना की जाती है।
कई रासायनिक प्रक्रियाओं के लिए पर्यावरण की अम्लता महत्वपूर्ण है, और किसी विशेष प्रतिक्रिया के होने या परिणाम की संभावना अक्सर पर्यावरण के पीएच पर निर्भर करती है। प्रयोगशाला अध्ययन या उत्पादन में प्रतिक्रिया प्रणाली में एक निश्चित पीएच मान बनाए रखने के लिए, बफर समाधान का उपयोग किया जाता है जो आपको पतला होने पर या जब एसिड या क्षार की थोड़ी मात्रा को समाधान में जोड़ा जाता है तो व्यावहारिक रूप से स्थिर पीएच मान बनाए रखने की अनुमति देता है।
विभिन्न जैविक मीडिया (तालिका 2) के एसिड-बेस गुणों को चिह्नित करने के लिए पीएच मान का व्यापक रूप से उपयोग किया जाता है।
जीवित प्रणालियों में होने वाली जैव रासायनिक प्रतिक्रियाओं के लिए प्रतिक्रिया माध्यम की अम्लता का विशेष महत्व है। एक समाधान में हाइड्रोजन आयनों की एकाग्रता अक्सर भौतिक रासायनिक गुणों और प्रोटीन और न्यूक्लिक एसिड की जैविक गतिविधि को प्रभावित करती है, इसलिए एसिड-बेस होमियोस्टेसिस को बनाए रखना शरीर के सामान्य कामकाज के लिए असाधारण महत्व का कार्य है। बफर सिस्टम की कार्रवाई के माध्यम से जैविक तरल पदार्थों के इष्टतम पीएच का गतिशील रखरखाव प्राप्त किया जाता है।
3) एक विशेष उपकरण का उपयोग - एक पीएच मीटर - आपको संकेतकों का उपयोग करने की तुलना में एक विस्तृत श्रृंखला में और अधिक सटीक (0.01 पीएच इकाइयों तक) पीएच को मापने की अनुमति देता है, सुविधाजनक और अत्यधिक सटीक है, आपको अपारदर्शी के पीएच को मापने की अनुमति देता है और रंगीन समाधान और इसलिए व्यापक रूप से उपयोग किया जाता है।
पीएच मीटर का उपयोग करके, आक्रामक वातावरण सहित तकनीकी प्रक्रियाओं की निरंतर निगरानी के लिए समाधान, पेयजल, खाद्य उत्पादों और कच्चे माल, पर्यावरणीय वस्तुओं और उत्पादन प्रणालियों में हाइड्रोजन आयनों (पीएच) की एकाग्रता को मापा जाता है।
यूरेनियम और प्लूटोनियम पृथक्करण समाधानों के पीएच की हार्डवेयर निगरानी के लिए एक पीएच मीटर अपरिहार्य है, जब इसके अंशांकन के बिना उपकरण रीडिंग की शुद्धता की आवश्यकताएं बहुत अधिक हैं।
उपकरण का उपयोग स्थिर और मोबाइल प्रयोगशालाओं में किया जा सकता है, जिसमें फील्ड प्रयोगशालाएं, साथ ही नैदानिक नैदानिक, फोरेंसिक, अनुसंधान, औद्योगिक, मांस और डेयरी और बेकिंग उद्योग शामिल हैं।
हाल ही में, मछलीघर के खेतों, घरेलू जल गुणवत्ता नियंत्रण, कृषि (विशेष रूप से हाइड्रोपोनिक्स में), और स्वास्थ्य निदान की निगरानी के लिए भी पीएच मीटर का व्यापक रूप से उपयोग किया गया है।
तालिका 2. कुछ जैविक प्रणालियों और अन्य समाधानों के लिए पीएच मान
|
सिस्टम (समाधान) | |
|
ग्रहणी | |
|
आमाशय रस | |
|
मानव रक्त | |
|
माँसपेशियाँ | |
|
अग्नाशय रस | |
|
कोशिका प्रोटोप्लाज्म | |
|
छोटी आंत | |
|
समुद्र का पानी | |
|
चिकन अंडे का सफेद | |
|
संतरे का रस | |
|
टमाटर का रस | |
पीएच मान और पीने के पानी की गुणवत्ता पर इसका प्रभाव।
पीएच क्या है?
पीएच("पोटेंशिया हाइड्रोजनी" - हाइड्रोजन की ताकत, या "पोंडस हाइड्रोजनी" - हाइड्रोजन का वजन) किसी भी पदार्थ में हाइड्रोजन आयनों की गतिविधि के मापन की एक इकाई है, मात्रात्मक रूप से इसकी अम्लता को व्यक्त करता है।
यह शब्द डेनमार्क में बीसवीं सदी की शुरुआत में दिखाई दिया। पीएच इंडेक्स को डेनिश केमिस्ट सोरेन पेट्र लॉरिट्ज सोरेनसेन (1868-1939) द्वारा पेश किया गया था, हालांकि उनके पूर्ववर्तियों में भी एक निश्चित "पानी की शक्ति" के बारे में बयान हैं।
हाइड्रोजन गतिविधि को हाइड्रोजन आयनों की सांद्रता के ऋणात्मक दशमलव लघुगणक के रूप में परिभाषित किया जाता है, जिसे मोल प्रति लीटर में व्यक्त किया जाता है:
पीएच = -लॉग
सादगी और सुविधा के लिए, गणना में पीएच को शामिल किया गया था। पीएच पानी में एच + और ओएच-आयनों के मात्रात्मक अनुपात से निर्धारित होता है, जो पानी के पृथक्करण के दौरान बनते हैं। पीएच स्तर को 14 अंकों के पैमाने पर मापने की प्रथा है।
यदि जल में हाइड्रॉक्साइड आयनों [OH-] की तुलना में मुक्त हाइड्रोजन आयनों (pH 7 से अधिक) की मात्रा कम है, तो जल में होगा क्षारीय प्रतिक्रिया, और एच + आयनों की बढ़ी हुई सामग्री के साथ (7 से कम पीएच) - एसिड प्रतिक्रिया. पूरी तरह शुद्ध आसुत जल में, ये आयन एक दूसरे को संतुलित करेंगे।
अम्लीय वातावरण: >
तटस्थ वातावरण: =
क्षारीय वातावरण: >
जब किसी विलयन में दोनों प्रकार के आयनों की सांद्रता समान होती है, तो विलयन को उदासीन कहा जाता है। उदासीन जल में pH 7 होता है।
जब विभिन्न रसायनों को पानी में घोला जाता है, तो यह संतुलन बदल जाता है, जिससे पीएच मान में परिवर्तन होता है। जब एसिड को पानी में जोड़ा जाता है, तो हाइड्रोजन आयनों की सांद्रता बढ़ जाती है, और हाइड्रॉक्साइड आयनों की सांद्रता तदनुसार कम हो जाती है, जब क्षार जोड़ा जाता है, इसके विपरीत, हाइड्रॉक्साइड आयनों की सामग्री बढ़ जाती है, और हाइड्रोजन आयनों की सांद्रता कम हो जाती है।
पीएच संकेतक पर्यावरण की अम्लता या क्षारीयता की डिग्री को दर्शाता है, जबकि "अम्लता" और "क्षारीयता" पानी में पदार्थों की मात्रात्मक सामग्री की विशेषता है जो क्रमशः क्षार और एसिड को बेअसर कर सकती है। सादृश्य के रूप में, हम तापमान के साथ एक उदाहरण दे सकते हैं, जो किसी पदार्थ के ताप की डिग्री को दर्शाता है, लेकिन ऊष्मा की मात्रा को नहीं। पानी में हाथ डुबाकर हम बता सकते हैं कि पानी ठंडा है या गर्म, लेकिन साथ ही हम यह भी पता नहीं लगा पाएंगे कि उसमें कितनी गर्मी है (यानी अपेक्षाकृत बोलें तो यह पानी कितनी देर में ठंडा होगा) ).
पीएच को पीने के पानी की गुणवत्ता के सबसे महत्वपूर्ण संकेतकों में से एक माना जाता है। यह एसिड-बेस बैलेंस दिखाता है और यह प्रभावित करता है कि रासायनिक और जैविक प्रक्रियाएं कैसे आगे बढ़ेंगी। पीएच मान के आधार पर, रासायनिक प्रतिक्रियाओं की दर, पानी के क्षरण की डिग्री, प्रदूषकों की विषाक्तता आदि में परिवर्तन हो सकता है। हमारी भलाई, मनोदशा और स्वास्थ्य सीधे हमारे शरीर के वातावरण के अम्ल-क्षार संतुलन पर निर्भर करते हैं।
आधुनिक मनुष्य प्रदूषित वातावरण में रहता है। बहुत से लोग अर्ध-तैयार उत्पादों से बने भोजन को खरीदते और खाते हैं। इसके अलावा, लगभग हर व्यक्ति दैनिक आधार पर तनाव के संपर्क में आता है। यह सब शरीर के वातावरण के अम्ल-क्षार संतुलन को प्रभावित करता है, इसे अम्ल की ओर स्थानांतरित करता है। चाय, कॉफी, बीयर, कार्बोनेटेड पेय शरीर में पीएच को कम करते हैं।
यह माना जाता है कि एक अम्लीय वातावरण कोशिका विनाश और ऊतक क्षति, रोगों के विकास और उम्र बढ़ने की प्रक्रिया और रोगजनकों के विकास के मुख्य कारणों में से एक है। एक अम्लीय वातावरण में, निर्माण सामग्री कोशिकाओं तक नहीं पहुंच पाती है, झिल्ली नष्ट हो जाती है।
बाह्य रूप से, किसी व्यक्ति के रक्त के अम्ल-क्षार संतुलन की स्थिति का अंदाजा उसकी आंखों के कोनों में उसके कंजाक्तिवा के रंग से लगाया जा सकता है। एक इष्टतम एसिड-बेस बैलेंस के साथ, कंजंक्टिवा का रंग चमकीला गुलाबी होता है, लेकिन अगर किसी व्यक्ति में रक्त की क्षारीयता बढ़ जाती है, तो कंजंक्टिवा गहरे गुलाबी रंग का हो जाता है, और अम्लता में वृद्धि के साथ, कंजंक्टिवा का रंग बन जाता है। फीका गुलाबी। इसके अलावा, कंजंक्टिवा का रंग एसिड-बेस बैलेंस को प्रभावित करने वाले पदार्थों के उपयोग के 80 सेकंड बाद ही बदल जाता है।
शरीर एक निश्चित स्तर पर मूल्यों को बनाए रखते हुए, आंतरिक तरल पदार्थों के पीएच को नियंत्रित करता है। शरीर का अम्ल-क्षार संतुलन अम्ल और क्षार का एक निश्चित अनुपात है जो इसके सामान्य कामकाज में योगदान देता है। एसिड-बेस बैलेंस शरीर के ऊतकों में इंटरसेलुलर और इंट्रासेल्युलर पानी के बीच अपेक्षाकृत स्थिर अनुपात बनाए रखने पर निर्भर करता है। यदि शरीर में तरल पदार्थ का अम्ल-क्षार संतुलन लगातार बनाए नहीं रखा जाता है, तो सामान्य कामकाज और जीवन का संरक्षण असंभव हो जाएगा। इसलिए, आप जो खाते हैं उसे नियंत्रित करना महत्वपूर्ण है।

अम्ल-क्षार संतुलन हमारे स्वास्थ्य का सूचक है। हम जितने अधिक अम्लीय होते हैं, उतनी ही जल्दी हमारी उम्र बढ़ती है और हम उतने ही अधिक बीमार होते हैं। सभी आंतरिक अंगों के सामान्य कामकाज के लिए, शरीर में पीएच स्तर 7 से 9 की सीमा में क्षारीय होना चाहिए।
हमारे शरीर के अंदर का पीएच हमेशा एक समान नहीं होता है - कुछ भाग अधिक क्षारीय होते हैं और कुछ अधिक अम्लीय होते हैं। शरीर केवल कुछ मामलों में ही पीएच होमियोस्टेसिस को नियंत्रित और बनाए रखता है, जैसे कि रक्त पीएच। गुर्दे और अन्य अंगों का पीएच स्तर, जिसका अम्ल-क्षार संतुलन शरीर द्वारा नियंत्रित नहीं किया जाता है, हमारे द्वारा उपभोग किए जाने वाले भोजन और पेय से प्रभावित होता है।
रक्त पीएच
रक्त पीएच स्तर शरीर द्वारा 7.35-7.45 की सीमा में बनाए रखा जाता है। मानव रक्त का सामान्य पीएच 7.4-7.45 होता है। इस सूचक में थोड़ा सा भी विचलन रक्त की ऑक्सीजन ले जाने की क्षमता को प्रभावित करता है। यदि रक्त का पीएच 7.5 तक बढ़ जाता है, तो यह 75% अधिक ऑक्सीजन वहन करता है। रक्त पीएच में 7.3 की कमी के साथ, किसी व्यक्ति के लिए बिस्तर से बाहर निकलना पहले से ही मुश्किल है। 7.29 पर, वह कोमा में पड़ सकता है, यदि रक्त का पीएच 7.1 से नीचे चला जाता है, तो व्यक्ति की मृत्यु हो जाती है।
रक्त पीएच को स्वस्थ श्रेणी में बनाए रखा जाना चाहिए, इसलिए शरीर इसे स्थिर रखने के लिए अंगों और ऊतकों का उपयोग करता है। नतीजतन, क्षारीय या अम्लीय पानी के सेवन से रक्त का पीएच स्तर नहीं बदलता है, लेकिन रक्त के पीएच को समायोजित करने के लिए शरीर के ऊतकों और अंगों का उपयोग उनके पीएच को बदल देता है।
गुर्दा पीएच
गुर्दे का पीएच पैरामीटर शरीर में पानी, भोजन और चयापचय प्रक्रियाओं से प्रभावित होता है। अम्लीय खाद्य पदार्थ (जैसे मांस, डेयरी, आदि) और पेय (मीठा सोडा, मादक पेय, कॉफी, आदि) गुर्दे में पीएच स्तर को कम करते हैं क्योंकि शरीर मूत्र के माध्यम से अतिरिक्त अम्लता को बाहर निकालता है। मूत्र का पीएच जितना कम होता है, किडनी के लिए काम करना उतना ही कठिन होता है। इसलिए, ऐसे खाद्य और पेय पदार्थों से गुर्दे पर एसिड लोड को संभावित एसिड-रीनल लोड कहा जाता है।
क्षारीय पानी के उपयोग से किडनी को लाभ होता है - मूत्र के पीएच स्तर में वृद्धि होती है, शरीर पर एसिड का भार कम होता है। मूत्र का पीएच बढ़ने से पूरे शरीर का पीएच बढ़ जाता है और गुर्दे को अम्लीय विषाक्त पदार्थों से छुटकारा मिलता है।
पेट का पीएच
एक खाली पेट में पिछले भोजन में उत्पादित एक चम्मच से अधिक पेट का एसिड नहीं होता है। खाना खाते समय पेट में जरूरत के हिसाब से एसिड बनता है। जब कोई व्यक्ति पानी पीता है तो पेट से एसिड नहीं निकलता है।
खाली पेट पानी पीना बहुत फायदेमंद होता है। पीएच उसी समय 5-6 के स्तर तक बढ़ जाता है। बढ़े हुए पीएच का हल्का एंटासिड प्रभाव होगा और लाभकारी प्रोबायोटिक्स (फायदेमंद बैक्टीरिया) में वृद्धि होगी। पेट का पीएच बढ़ने से शरीर का पीएच बढ़ जाता है, जिससे पाचन क्रिया स्वस्थ रहती है और अपच के लक्षणों से राहत मिलती है।
चमड़े के नीचे का वसा पीएच
शरीर के वसायुक्त ऊतकों में एक अम्लीय पीएच होता है क्योंकि उनमें अतिरिक्त एसिड जमा होते हैं। शरीर को एसिड को वसायुक्त ऊतकों में जमा करना पड़ता है जब इसे अन्य तरीकों से हटाया या बेअसर नहीं किया जा सकता है। इसलिए, शरीर के पीएच में एसिड पक्ष में बदलाव अतिरिक्त वजन के कारकों में से एक है।
क्षारीय पानी का शरीर के वजन पर सकारात्मक प्रभाव यह है कि क्षारीय पानी ऊतकों से अतिरिक्त एसिड को हटाने में मदद करता है, क्योंकि यह गुर्दे को अधिक कुशलता से काम करने में मदद करता है। यह वजन को नियंत्रित करने में मदद करता है, क्योंकि शरीर को "स्टोर" करने वाले एसिड की मात्रा बहुत कम हो जाती है। क्षारीय पानी वजन घटाने के दौरान फैटी टिशू द्वारा उत्पादित अतिरिक्त एसिड से निपटने में शरीर की मदद करके स्वस्थ आहार और व्यायाम के परिणामों को भी बढ़ाता है।
हड्डियाँ
हड्डियों में एक क्षारीय पीएच होता है क्योंकि वे ज्यादातर कैल्शियम से बने होते हैं। उनका पीएच स्थिर है, लेकिन अगर रक्त को पीएच समायोजन की आवश्यकता होती है, तो हड्डियों से कैल्शियम लिया जाता है।
क्षारीय पानी हड्डियों को जो लाभ पहुंचाता है, वह शरीर को एसिड की मात्रा को कम करके उनकी रक्षा करना है। अध्ययनों से पता चला है कि क्षारीय पानी पीने से हड्डियों का पुनर्जीवन कम हो जाता है - ऑस्टियोपोरोसिस।
जिगर पीएच
लिवर में थोड़ा क्षारीय पीएच होता है, जो भोजन और पेय दोनों से प्रभावित होता है। चीनी और अल्कोहल को लीवर में टूटना चाहिए, और इससे अतिरिक्त एसिड बनता है।
जिगर के लिए क्षारीय पानी के लाभ ऐसे पानी में एंटीऑक्सिडेंट की उपस्थिति है; यह पाया गया है कि क्षारीय पानी यकृत में स्थित दो एंटीऑक्सीडेंट के काम को बढ़ाता है, जो अधिक प्रभावी रक्त शोधन में योगदान देता है।
शरीर पीएच और क्षारीय पानी
क्षारीय पानी शरीर के उन हिस्सों को अनुमति देता है जो रक्त के पीएच को अधिक कुशलता से काम करने के लिए बनाए रखते हैं। रक्त पीएच को बनाए रखने के लिए जिम्मेदार शरीर के हिस्सों में पीएच स्तर बढ़ाने से इन अंगों को स्वस्थ रहने और कुशलतापूर्वक कार्य करने में मदद मिलेगी।
भोजन के बीच, आप क्षारीय पानी पीकर अपने शरीर को पीएच संतुलन में मदद कर सकते हैं। पीएच में थोड़ी सी भी वृद्धि स्वास्थ्य पर भारी प्रभाव डाल सकती है।
जापानी वैज्ञानिकों के शोध के अनुसार, पीने के पानी का पीएच, जो 7-8 की सीमा में है, जनसंख्या की जीवन प्रत्याशा को 20-30% तक बढ़ा देता है।
पीएच स्तर के आधार पर, पानी को कई समूहों में विभाजित किया जा सकता है:
दृढ़ता से अम्लीय पानी< 3
अम्लीय पानी 3 - 5
थोड़ा अम्लीय जल 5 - 6.5
तटस्थ जल 6.5 - 7.5
थोड़ा क्षारीय पानी 7.5 - 8.5
क्षारीय पानी 8.5 - 9.5
अत्यधिक क्षारीय पानी> 9.5
आमतौर पर, पीने के नल के पानी का पीएच स्तर उस सीमा के भीतर होता है जिस पर यह पानी की उपभोक्ता गुणवत्ता को सीधे प्रभावित नहीं करता है। नदी के पानी में पीएच आमतौर पर 6.5-8.5 के भीतर होता है, वायुमंडलीय वर्षा में 4.6-6.1, दलदलों में 5.5-6.0, समुद्री जल में 7.9-8.3 होता है।
डब्ल्यूएचओ पीएच के लिए चिकित्सकीय रूप से अनुशंसित कोई मूल्य प्रदान नहीं करता है। यह ज्ञात है कि कम पीएच पर, पानी अत्यधिक संक्षारक होता है, और उच्च स्तर (पीएच> 11) पर, पानी एक विशिष्ट साबुन जैसा, एक अप्रिय गंध प्राप्त करता है, और आंख और त्वचा में जलन पैदा कर सकता है। इसीलिए पीने और घरेलू पानी के लिए 6 से 9 की सीमा में पीएच स्तर को इष्टतम माना जाता है।
|
|||||||||||||||||||||||||||||||||||||||||||||||



जानना दिलचस्प:जर्मन बायोकेमिस्ट ओटो वारबर्ग, जिन्हें 1931 में फिजियोलॉजी या मेडिसिन में नोबेल पुरस्कार से सम्मानित किया गया था, ने साबित किया कि ऑक्सीजन की कमी (एक अम्लीय पीएच)<7.0) в тканях приводит к изменению нормальных клеток в злокачественные.
वैज्ञानिक ने पाया कि कैंसर कोशिकाएं 7.5 और उससे अधिक पीएच मान वाले मुक्त ऑक्सीजन से संतृप्त वातावरण में विकसित होने की अपनी क्षमता खो देती हैं! इसका मतलब यह है कि जब शरीर में तरल पदार्थ अम्लीय हो जाते हैं, तो कैंसर के विकास को बढ़ावा मिलता है।
पिछली शताब्दी के 60 के दशक में उनके अनुयायियों ने साबित कर दिया कि कोई भी रोगजनक वनस्पति पीएच = 7.5 और उससे अधिक पर गुणा करने की क्षमता खो देती है, और हमारी प्रतिरक्षा प्रणाली आसानी से किसी भी आक्रमणकारियों का सामना कर सकती है!
स्वास्थ्य को बनाए रखने और बनाए रखने के लिए, हमें उचित क्षारीय पानी (pH = 7.5 और ऊपर) की आवश्यकता होती है।यह आपको शरीर के तरल पदार्थों के अम्ल-क्षार संतुलन को बेहतर बनाए रखने की अनुमति देगा, क्योंकि मुख्य जीवित वातावरण में थोड़ी क्षारीय प्रतिक्रिया होती है।
पहले से ही एक तटस्थ जैविक वातावरण में, शरीर में खुद को ठीक करने की अद्भुत क्षमता हो सकती है।

पता नहीं कहाँ मिलेगा सही पानी ? मैं संकेत दूंगा!

टिप्पणी:
बटन दबाना" जानना» कोई वित्तीय खर्च और दायित्व नहीं होता है।
आप ही केवल हैं अपने क्षेत्र में सही पानी की उपलब्धता के बारे में जानकारी प्राप्त करें,
साथ ही नि:शुल्क स्वस्थ लोगों के क्लब का सदस्य बनने का अनूठा अवसर प्राप्त करें
और सभी ऑफ़र + संचयी बोनस पर 20% की छूट प्राप्त करें।

अंतर्राष्ट्रीय स्वास्थ्य क्लब कोरल क्लब में शामिल हों, मुफ़्त डिस्काउंट कार्ड प्राप्त करें, पदोन्नति में भाग लेने का अवसर, संचयी बोनस और अन्य विशेषाधिकार प्राप्त करें!

हाइड्रोजन इंडेक्स, पीएच (उच्चारण "पीश", अंग्रेजी पीएच का अंग्रेजी उच्चारण - piː "eɪtʃ," pee ") - एक समाधान में हाइड्रोजन आयनों की गतिविधि का एक उपाय (बहुत पतला समाधान में यह एकाग्रता के बराबर है), और मात्रात्मक रूप से व्यक्त करता है इसकी अम्लता की गणना हाइड्रोजन आयनों की गतिविधि के दसवें लघुगणक के ऋणात्मक (रिवर्स साइन) लघुगणक के रूप में की जाती है, जिसे मोल प्रति लीटर में व्यक्त किया जाता है: कहानी यह अवधारणा 1909 में डेनिश रसायनज्ञ सोरेनसेन द्वारा पेश की गई थी। सूचक को पीएच कहा जाता है, लैटिन शब्द पोटेंशिया हाइड्रोजनी के पहले अक्षर के बाद - हाइड्रोजन की ताकत, या पोंडस हाइड्रोजनी - हाइड्रोजन का वजन। सामान्य तौर पर, रसायन विज्ञान में, संयोजन pX का उपयोग आमतौर पर -lg X के बराबर मान को दर्शाने के लिए किया जाता है, और इस मामले में अक्षर H हाइड्रोजन आयनों (H +) की सांद्रता को दर्शाता है, या, अधिक सटीक रूप से, हाइड्रोनियम की थर्मोडायनामिक गतिविधि आयन। पीएच और पीओएच से संबंधित समीकरण पीएच मान आउटपुट 25 ° C पर शुद्ध पानी में, हाइड्रोजन आयनों () और हाइड्रॉक्साइड आयनों () की सांद्रता समान होती है और 10 −7 mol / l की मात्रा होती है, यह सीधे पानी के आयन उत्पाद की परिभाषा से होता है, जो बराबर है और 10 −14 मोल² / एल² (25 डिग्री सेल्सियस पर) है। जब किसी विलयन में दोनों प्रकार के आयनों की सांद्रता समान होती है, तो विलयन को उदासीन कहा जाता है। जब एसिड को पानी में जोड़ा जाता है, तो हाइड्रोजन आयनों की सांद्रता बढ़ जाती है, और हाइड्रॉक्साइड आयनों की सांद्रता तदनुसार घट जाती है, जब एक आधार जोड़ा जाता है, इसके विपरीत, हाइड्रॉक्साइड आयनों की सामग्री बढ़ जाती है, और हाइड्रोजन आयनों की सांद्रता कम हो जाती है। कब > वे कहते हैं कि समाधान अम्लीय है, और कब > - क्षारीय। प्रस्तुति की सुविधा के लिए, नकारात्मक घातांक से छुटकारा पाने के लिए, हाइड्रोजन आयनों की सांद्रता के बजाय, उनके दशमलव लघुगणक का उपयोग विपरीत चिह्न के साथ किया जाता है, जो वास्तव में हाइड्रोजन सूचक है - पीएच। पोह पारस्परिक पीएच मान कुछ कम व्यापक हो गया है - समाधान की मूलभूतता का एक संकेतक, पीओएच, ओएच - आयनों के समाधान में एकाग्रता के नकारात्मक दशमलव लघुगणक के बराबर: 25 डिग्री सेल्सियस पर किसी भी जलीय घोल की तरह, यह स्पष्ट है कि इस तापमान पर: विभिन्न अम्लता के समाधान में पीएच मान
- लोकप्रिय धारणा के विपरीत, पीएच न केवल 0 से 14 की सीमा में भिन्न हो सकता है, बल्कि इन सीमाओं से परे भी जा सकता है। उदाहरण के लिए, हाइड्रोजन आयनों की सांद्रता = 10 −15 mol / l, pH = 15, 10 mol / l pOH = −1 के हाइड्रॉक्साइड आयनों की सांद्रता पर।
|
- हाइड्रोजन आयनों की सांद्रता के मोटे अनुमान के लिए, एसिड-बेस संकेतकों का व्यापक रूप से उपयोग किया जाता है - कार्बनिक डाई पदार्थ, जिसका रंग माध्यम के पीएच पर निर्भर करता है। सबसे प्रसिद्ध संकेतकों में लिटमस, फिनोलफथेलिन, मिथाइल ऑरेंज (मिथाइल ऑरेंज) और अन्य शामिल हैं। संकेतक दो अलग-अलग रंगीन रूपों में मौजूद हो सकते हैं, या तो अम्लीय या बुनियादी। प्रत्येक संकेतक का रंग परिवर्तन इसकी अम्लता सीमा में होता है, आमतौर पर 1-2 इकाइयाँ।
- पीएच माप की कार्य सीमा का विस्तार करने के लिए, तथाकथित सार्वभौमिक संकेतक का उपयोग किया जाता है, जो कई संकेतकों का मिश्रण है। एक अम्लीय से क्षारीय क्षेत्र में जाने पर सार्वभौमिक संकेतक लगातार लाल से पीले, हरे, नीले से बैंगनी रंग में बदलता है। सांकेतिक विधि द्वारा pH का निर्धारण मेघमय या रंगीन विलयनों के लिए कठिन होता है।
- एक विशेष उपकरण का उपयोग - एक पीएच मीटर - आपको संकेतकों की तुलना में पीएच को एक विस्तृत श्रृंखला में और अधिक सटीक (0.01 पीएच इकाइयों तक) मापने की अनुमति देता है। पीएच का निर्धारण करने के लिए आयनोमेट्रिक विधि एक गैल्वेनिक सर्किट के ईएमएफ को मापने पर आधारित है, जिसमें एक विशेष ग्लास इलेक्ट्रोड शामिल है, जिसमें एक विशेष ग्लास इलेक्ट्रोड शामिल है, जिसकी क्षमता आसपास के समाधान में एच + आयनों की एकाग्रता पर निर्भर करती है। विधि सुविधाजनक और अत्यधिक सटीक है, विशेष रूप से चयनित पीएच रेंज में संकेतक इलेक्ट्रोड को कैलिब्रेट करने के बाद, आपको अपारदर्शी और रंगीन समाधानों के पीएच को मापने की अनुमति मिलती है, और इसलिए इसका व्यापक रूप से उपयोग किया जाता है।
- विश्लेषणात्मक वॉल्यूमेट्रिक विधि - एसिड-बेस अनुमापन - समाधान की अम्लता का निर्धारण करने के लिए सटीक परिणाम भी देता है। परीक्षण विलयन में ज्ञात सान्द्रता (टाइट्रेट) का विलयन बूंद-बूंद करके डाला जाता है। जब वे मिश्रित होते हैं, तो एक रासायनिक प्रतिक्रिया होती है। तुल्यता बिंदु - वह क्षण जब टाइट्रेंट पूरी तरह से प्रतिक्रिया को पूरा करने के लिए पर्याप्त होता है - एक संकेतक का उपयोग करके तय किया जाता है। इसके अलावा, जोड़ा टाइट्रेंट समाधान की एकाग्रता और मात्रा को जानने के बाद, समाधान की अम्लता की गणना की जाती है।
- पीएच मानों पर तापमान का प्रभाव
SanPinN के नियमों के अनुसार, हाइड्रोजन आयनों की सांद्रता द्वारा निर्धारित एसिड-बेस संकेतकों की डिग्री, पीएच पैरामीटर बनाती है, जो आम तौर पर पीने के पानी के लिए 6-9 इकाइयां होती हैं। इस सूचक के अनुसार, रूसी मानक लगभग यूरोपीय संघ के निर्देश - 6.50-9.50 और अमेरिकी पर्यावरण संरक्षण एजेंसी (यूएसईपीए) की आवश्यकताओं - 6.50-8.50 से भिन्न नहीं हैं।
इसी समय, विभिन्न औद्योगिक जरूरतों के लिए पानी के पीएच मानदंड पीने के पानी के पीएच मानदंडों से भिन्न होते हैं। उदाहरण के लिए:
- हाइड्रोपोनिक्स में, 5.50-7.50 के स्तर वाले समाधानों का उपयोग किया जाता है और इस श्रेणी को विशिष्ट पौधों की प्रजातियों के आधार पर संकरे खंडों में विभाजित किया जाता है,
- सार्वजनिक पूल में यह मानक 7.20-7.40 है; निजी व्यापक में - 7.20-7.60; डीआईएन 19643-1 - 6.50-7.60 के अनुसार,
- बियर के उत्पादन में, 6.00-6.50 के संकेतक वाले जल आधार का उपयोग किया जाता है,
- शीतल पेय के लिए - 3.00-6.00,
- निर्यात वोदका के लिए, संकेतक प्रक्रिया के पानी की कठोरता पर निर्भर करता है - और 0 से 0.60 meq/l और 6.50 - 0.61-1.2 meq/l पर कठोरता के साथ 7 के बराबर है; "घरेलू बाजार" में वोडका - pH<7,80,
- रासायनिक फाइबर उत्पादन में - 7.00-8.00,
- रंगाई और परिष्करण में - 6.50-8.50,
- गर्मी आपूर्ति प्रणालियों में, पैरामीटर +25ºС के तापमान पर इंगित किया जाता है और खुले सिस्टम के लिए 7.00-8.50 की सीमा में और बंद लोगों के लिए 7.00-11.00 के भीतर होता है,
- पावर इंजीनियरिंग और स्टीम बॉयलरों में - 8.50 से कम नहीं,
- शीतलन प्रणालियों में: परिसंचारी और अतिरिक्त पानी के लिए - 6.50-8.50, संचलन कोल्ड सर्किट में - 6.50-8.20, गर्म सर्किट - 6.80-8.00, आदि।
पीएच के स्तर और निर्भरता का निर्धारण
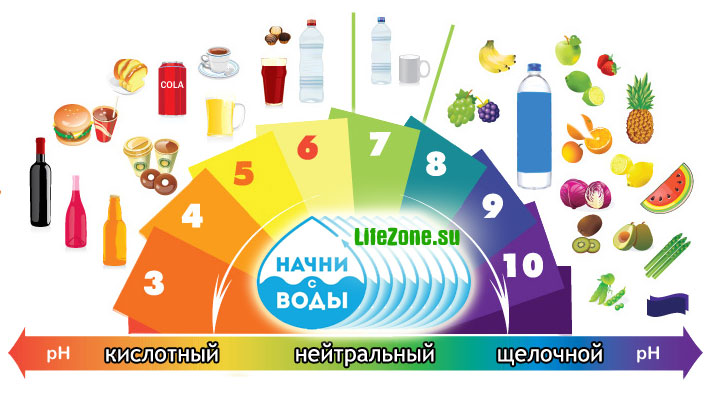
एसिड-बेस पर्यावरण की प्रकृति का निर्धारण करने के लिए पैमाने में 14 इकाइयां होती हैं, जहां पीएच = 7 का औसत मूल्य तटस्थ माना जाता है। इस पैमाने के साथ शुरुआत (शून्य तक) में बदलाव के साथ, समाधान अम्लीय हो जाते हैं। अंत में स्थानांतरित होने पर - क्षार की प्रकृति। सबसे अधिक बार, इस तरह की निर्भरता लगातार उन्नयन के साथ तालिकाओं में परिलक्षित होती है:

तुलना के लिए, GOST 6709-96 के अनुसार, पीएच डिस्टिलेट का मान 5.40-6.60 की सीमा में हो सकता है।
चूंकि हाइड्रोजन आयनों की सांद्रता कम है (एक तटस्थ माध्यम के लिए यह दशमलव बिंदु के बाद सात शून्य है), संकेतक को अधिक परिचित रूप में एक नकारात्मक दशमलव लघुगणक के रूप में व्यक्त किया जाता है। तालिकाओं में, "पीएच, इकाइयां" आमतौर पर माप की इकाइयों के रूप में लिखी जाती हैं। या µg/l (माइक्रोग्राम प्रति लीटर)।
पीएच मान कुल क्षारीयता (पानी की क्षारीयता) से भिन्न होता है, जिसे mg-eq/l में व्यक्त किया जाता है, जो पानी में कमजोर एसिड के हाइड्रॉक्सिल आयनों/आयनों के योग से निर्धारित होता है। कम क्षारीयता बाहरी कारकों के प्रभाव में पीएच में तेज बदलाव को भड़काती है।
प्राकृतिक जल में, पीएच, ज्यादातर मामलों में, 6.50-8.50 की सीमा में है, जो एक ओर मुक्त कार्बन डाइऑक्साइड के अनुपात पर निर्भरता को दर्शाता है, और दूसरी ओर बाइकार्बोनेट आयन। दलदल के पानी में, पीएच मान कम होता है और अम्लता की ओर बढ़ता है। अक्सर यह पैरामीटर खुले जल निकायों में प्रदूषण का संकेतक बन जाता है, जो एसिड या क्षार की उच्च सामग्री वाले अपशिष्टों की उपस्थिति का प्रदर्शन करता है।
गहन प्रकाश संश्लेषण के साथ, जो गर्मियों में मनाया जाता है, संकेतक का स्तर 8.50-9.00 यूनिट तक बढ़ सकता है। इसके अलावा, पैरामीटर के मान लवण, हाइड्रॉक्साइड्स, हास्य पदार्थों आदि के हाइड्रोलिसिस के अधीन कार्बोनेट की एकाग्रता से प्रभावित होते हैं।
रोजमर्रा की जिंदगी में पीएच का महत्व
जापानी वैज्ञानिकों ने उन क्षेत्रों में उपभोक्ताओं का तुलनात्मक अध्ययन किया जहां वे पीने के पानी का उपयोग करते हैं, पीएच मान या तो अम्लता की ओर या क्षारीयता की ओर स्थानांतरित हो जाता है। उन्होंने निष्कर्ष निकाला कि जिन क्षेत्रों में यह सूचक औसत से ऊपर है, लोग देश में औसत जीवन प्रत्याशा से 20-30% अधिक जीवित रहते हैं। एक कथित कारण के रूप में, पैथोलॉजिकल माइक्रोफ्लोरा के विकास के लिए अम्लीय जल के अधिक से अधिक "आराम" को कहा जाता है।
इस तथ्य के कारण कि नल के पानी का वास्तव में मानव स्वास्थ्य पर महत्वपूर्ण प्रभाव पड़ता है, इसके संपर्क में आने वाले कुछ तकनीकी सामानों को एजेंटों के रूप में विज्ञापित किया जाने लगा है जो पानी के रासायनिक गुणों को बदल सकते हैं। उदाहरण के लिए, http://water-save.com/ सेवर्स को ऐसे उपकरणों के रूप में वर्णित किया जाता है जो "पानी को कमजोर आयनों से समृद्ध करते हैं जो चयापचय को सक्रिय करते हैं।" वास्तव में, केवल आर्थिक, लेकिन अर्थशास्त्री की स्थापना के "उपचार" प्रभाव की मज़बूती से पुष्टि नहीं की जाती है।
हालांकि, यह शरीर के लिए पीएच पैरामीटर के मान को नकारता नहीं है। प्रत्येक वातावरण - मानव शरीर के विभिन्न वातावरणों सहित - का अपना "पीएच-गाइड" होता है:
- लार - 6.8-7.4 (लार की उच्च दर के साथ - 7.8),
- आँसू - 7.3-7.5,
- रक्त - 7.43,
- लसीका - 7.5,
- मूत्र - 5.5 (रेंज 5.0-7.5), आदि।

विभिन्न माध्यमों की अम्ल-क्षार अवस्था को दृष्टिगत रूप से प्रदर्शित करने के लिए, तालिकाएँ हैं जिनमें मूल्यों को आरोही क्रम में व्यवस्थित किया गया है:



