Зависит от рн. Водородный показатель (pH-фактор)
В этой статье мы отвечаем на вопросы что такое кислотность вина и как ее определяют. Что такое pH и зачем его знать потребителю. Что такое градус алкоголя.
Градус алкоголя
Одно из этих сокращенией очень простое — ABV означает английское «alcohol by volume», те. содержание алкоголя (в нашем случае — этанола) в объёме жидкости. Обычно измеряется в процентах. А в разговорной речи называется градусом. Например, выражение сорокаградусная водка означает, что в предложенном растворе содержится 40% — сорок объёмных процентов алкоголя.
Объемный процент или градус измеряется в количестве милилитров «чистого» этанола в объеме 100 мл при температуре 20 градусов Цельсия.
В двух словах понятно, что если на бутылке указано ABV 5.5%, как, например, на некоторых винах Москато д’Асти, то это слабогазированное и слабоалкогольное вино можно легонько потягивать весь вечер не опасаясь заполучить назавтра похмельный синдром. Как говорится, в кефире алкоголя больше(с)!
Кстати, именно поэтому Москато д’Асти и другое итальянское игристое, Проссеко, так популярны на голливудских вечеринках. Все весь вечер ходят с бокалом в руке, а пьяных нет. И домой можно самому за рулем уехать. Хотя судя по новостям, участников этих вечеринок последнее соображение не очень волнует.
Немного теории — что такое pH
На интуитивном уровне мы все примерно понимаем, что такое кислотность. Степень «кислости», если так можно сказать. В химии же этот термин — кислотность, лат. aciditas, англ. acidity — обозначает характеристику активности ионов водорода в растворах и жидкостях.
Различают истинную (активную) и общую (титруемую) кислотность. В водных растворах неорганические вещества, т.е. соли, кислоты и щелочи (растворенные), разделяются на составляющие их ионы.
При этом положительнозаряженные ионы водорода H+ являются носителями кислотных свойств, а отрицательно заряженные ионы OH− (их еще называют гидроксилами) – носителями щелочных свойств.
Сто лет назад химиками был введен специальный водородный показатель, который принято обозначать символами рН .
Немного математики
Не-нудники(c) и не-математики(c) могут пропустить этот абзац. А для оставшихся сообщим, что для водных растворов действует уравнение равновесия — произведение активности ионов H+ и OH- постоянно. В так называемых нормальных условиях, т.е. при температуре воды 22°C и нормальном давлении, оно равно 10 в минус 14-ой степени.
Датский биохимик Серенсен в 1909 году ввел в обращение водородный показатель рН, по определению равный десятичному логарифму активности водородных ионов, взятому с минусом:
рН = - lg (активность Н+)
В нейтральной среде, как мы только что сказали, активности ионов равны, т.е. произведение активности H+ на активность OH- равна квадрату активности H+. И равна 10 в минус 14-ой степени.
Значит, после деления 14 на 2, отрицательный десятичный логарифм будет равен 7. Это означает, что (при температуре 22 °C) кислотность чистой воды, то есть нейтральная кислотность, равна семи единицам: pH = 7.
Растворы и жидкости считаются кислыми, если их pH меньше 7 , и щелочными, если больше.
Обычно изделия пищевой промышленности, включая вино, имеют, как правило, кислую реакцию. Щелочную реакцию имеют химические разрыхлители теста (сода, карбонат аммония) и изделия, приготовленные с их применением, например печенье и пряники.
Три вида кислотности
Вернемся к вину. Термин»кислотность» — один из самых употребимых при анализе, описании и производстве вин. Практически кислотность — одна из самых главных характеристик и химии вина, и вкуса. В виноделии различают три вида кислотности:
- общую или титруемую
- активную или истинную — это и есть [водородный] показатель активности pH
- летучую кислотность
Титруемая кислотность
Титруемая или общая кислотность определяет содержание в соке или вине всех свободных кислот и их кислых солей в совокупности.
Величина её определяется количеством щелочи (например, едкого натра или калия), необходимой для нейтрализации этих кислот. То есть такое количество щелочи, которое надо добавить в вино, чтобы получить из него абсолютно нейтральный раствор (pH=7.0).
Измеряется общая кислотность в граммах на литр.
Активная кислотность
Активная или истинная кислотность pH . Математически — это отрицательный логарифм концентрации водородных ионов, как было сказано выше. Технически, это наиболее точная характеристика кислотности вина.
Она зависит от количества наиболее сильных кислот содержащихся в вине. Сильными называются кислоты, имеющие наибольшую константу (Кд) диссоциации [кислоты].
Пример типичных кислот упорядоченных по «силе», то есть по убыванию константы диссоциации (степени кислоты):
- Лимонная Кд = 8.4 10-4
- Янтарная Кд = 7.4 10-4
- Яблочная Кд = 3.95 10-4
- Молочная Кd = 1.4 10-4
От величины рН зависит количественное соотношение первичных и вторичных продуктов брожения, склонность вина к окислению, кристаллическим и биологическим помутнениям, подверженность дефектам и сопротивляемость болезням вина.
Примеры
Простое объяснение логарифмической зависимости. Раствор с рН = 3 в десять раз более кислый, чем раствор с рН = 4. Или, более практический пример, вино с pH = 3.2 на 25% кислее вина с pH = 3.3.
При необходимости исправить кислотность вина, виноделы добавляют смесь 1.9 г/л молочной кислоты и 2.27 г/л винной (диоксиянтарной или тартаровой) кислоты. Это позволяет уменьшить pH приблизительного на 0.1 (в диапазоне от 3 до 4).
А если, например, вино получилось с pH=3.7 и винодел хочет его довести до pH=3.5, он увеличит эту «дозу» в два раза.
Величина рН для некоторых продуктов
В таблице ниже указаны величины кислотности некоторых распространенных продуктов и чистой воды при разной температуре:
| Продукт | Кислотность, рН |
| Лимонный сок | 2,1 |
| Вино, приблизительно | 3,5 |
| Томатный сок | 4,1 |
| Апельсиновый сок | 4,2 |
| Черный кофе | 5,0 |
| Чистая вода при 100 °С | 6,13 |
| Чистая вода при 50 °С | 6,63 |
| Свежее молоко | 6,68 |
| Чистая вода при 22 °С | 7,0 |
| Чистая вода при 0° С | 7,48 |
Летучая кислотность
Летучая кислотность (volatile acidity или, сокращенно, VA) – это та часть кислот в вине, которую можно уловить носом.
В отличие от тех кислот, которые ощутимы на вкус (о чем мы говорили выше).
Летучая кислотность, или иными словами, скисание вина — один из распространенных дефектов. Основные виновники его — уксусная кислота (пахнет уксусом) и её эфир – этилацетат (пахнет лаком для ногтей).
Бактерии, ответственные за летучую кислотность, активно развиваются в условиях низкой кислотности и высокого содержания сахаров. В малых концентрациях летучая кислотность придает вину пикантность. А при превышении порога уксусно-лаковая составляющая забивает полезные ароматы и портит вкус вина.
Водородный показатель – рН – это мера активности (в случае разбавленных растворов отражает концентрацию) ионов водорода в растворе, количественно выражающая его кислотность, вычисляется как отрицательный (взятый с обратным знаком) десятичный логарифм активности водородных ионов, выраженной в молях на литр.
pН = – lg
Это понятие было введено в 1909 году датским химиком Сёренсеном. Показатель называется pH, по первым буквам латинских слов potentia hydrogeni – сила водорода, или pondus hydrogenii – вес водорода.
Несколько меньшее распространение получила обратная pH величина – показатель основности раствора, pOH, равная отрицательному десятичному логарифму концентрации в растворе ионов OH:
рОН = – lg
В чистой воде при 25°C концентрации ионов водорода () и гидроксид-ионов () одинаковы и составляют 10 -7 моль/л, это напрямую следует из константы автопротолиза воды К w , которую иначе называют ионным произведением воды:
К w = · =10 –14 [моль 2 /л 2 ] (при 25°C)
рН + рОН = 14
Когда концентрации обоих видов ионов в растворе одинаковы, говорят, что раствор имеет нейтральную реакцию. При добавлении к воде кислоты концентрация ионов водорода увеличивается, а концентрация гидроксид-ионов соответственно уменьшается, при добавлении основания – наоборот, повышается содержание гидроксид-ионов, а концентрация ионов водорода падает. Когда > говорят, что раствор является кислым, а при > – щелочным.
Определение рН
Для определения значения pH растворов широко используют несколько способов.
1) Водородный показатель можно приблизительно оценивать с помощью индикаторов, точно измерять pH-метром или определять аналитически путём, проведением кислотно-основного титрования.
Для грубой оценки концентрации водородных ионов широко используются кислотно-основные индикаторы – органические вещества-красители, цвет которых зависит от pH среды. К наиболее известным индикаторам принадлежат лакмус, фенолфталеин, метиловый оранжевый (метилоранж) и другие. Индикаторы способны существовать в двух по-разному окрашенных формах – либо в кислотной, либо в основной. Изменение цвета каждого индикатора происходит в своём интервале кислотности, обычно составляющем 1-2 единицы (см. Таблица 1, занятие 2).
Для расширения рабочего интервала измерения pH используют так называемый универсальный индикатор, представляющий собой смесь из нескольких индикаторов. Универсальный индикатор последовательно меняет цвет с красного через жёлтый, зелёный, синий до фиолетового при переходе из кислой области в щелочную. Определения pH индикаторным методом затруднено для мутных или окрашенных растворов.
2) Аналитический объёмный метод – кислотно-основное титрование – также даёт точные результаты определения общей кислотности растворов. Раствор известной концентрации (титрант) по каплям добавляется к исследуемому раствору. При их смешивании протекает химическая реакции. Точка эквивалентности – момент, когда титранта точно хватает, чтобы полностью завершить реакцию, – фиксируется с помощью индикатора. Далее, зная концентрацию и объём добавленного раствора титранта, вычисляется общая кислотность раствора.
Кислотность среды имеет важное значение для множества химических процессов, и возможность протекания или результат той или иной реакции часто зависит от pH среды. Для поддержания определённого значения pH в реакционной системе при проведении лабораторных исследований или на производстве применяют буферные растворы, которые позволяют сохранять практически постоянное значение pH при разбавлении или при добавлении в раствор небольших количеств кислоты или щёлочи.
Водородный показатель pH широко используется для характеристики кислотно-основных свойств различных биологических сред (Табл. 2).
Кислотность реакционной среды особое значение имеет для биохимических реакций, протекающих в живых системах. Концентрация в растворе ионов водорода часто оказывает влияние на физико-химические свойства и биологическую активность белков и нуклеиновых кислот, поэтому для нормального функционирования организма поддержание кислотно-основного гомеостаза является задачей исключительной важности. Динамическое поддержание оптимального pH биологических жидкостей достигается благодаря действию буферных систем.
3) Использование специального прибора – pH-метра – позволяет измерять pH в более широком диапазоне и более точно (до 0,01 единицы pH), чем с помощью индикаторов, отличается удобством и высокой точностью, позволяет измерять pH непрозрачных и цветных растворов и потому широко используется.
С помощью рН-метра измеряют концентрацию ионов водорода (pH) в растворах, питьевой воде, пищевой продукции и сырье, объектах окружающей среды и производственных систем непрерывного контроля технологических процессов, в т. ч. в агрессивных средах.
рН-метр незаменим для аппаратного мониторинга pH растворов разделения урана и плутония, когда требования к корректности показаний аппаратуры без её калибровки чрезвычайно высоки.
Прибор может использоваться в лабораториях стационарных и передвижных, в том числе полевых, а также клинико-диагностических, судебно-медицинских, научно-исследовательских, производственных, в том числе мясо-молочной и хлебопекарной промышленности.
Последнее время pH-метры также широко используются в аквариумных хозяйствах, контроля качества воды в бытовых условиях, земледелия (особенно в гидропонике), а также – для контроля диагностики состояния здоровья.
Таблица 2. Значения рН для некоторых биологических систем и других растворов
|
Система (раствор) | |
|
Двенадцатиперстная кишка | |
|
Желудочный сок | |
|
Кровь человека | |
|
Мышечная ткань | |
|
Панкреатический сок | |
|
Протоплазма клеток | |
|
Тонкая кишка | |
|
Морская вода | |
|
Белок куриного яйца | |
|
Апельсиновый сок | |
|
Томатный сок | |
Показатель pH и его влияние на качество питьевой воды.
Что такое pH?
pH («potentia hydrogeni» - сила водорода, или «pondus hydrogenii» - вес водорода) - это единица измерения активности ионов водорода в любом веществе, количественно выражающая его кислотность.
Данный термин появился в начале ХХ века в Дании. Показатель pH ввел датский химик Сорен Петр Лауриц Соренсен (1868-1939), хотя утверждения о некой «силе воды» встречаются и у его предшественников.
Активность водорода определяется как отрицательный десятичный логарифм концентрации водородных ионов, выраженной в молях на литр:
pH = -log
Для простоты и удобства при вычислениях был введен показатель pH. рН определяется количественным соотношением в воде ионов Н+ и ОН-, образующихся при диссоциации воды. Принято измерять уровень pH по 14-цифровой шкале.
Если в воде пониженное содержание свободных ионов водорода (рН больше 7) по сравнению с ионами гидроксида [ОН-], то вода будет иметь щелочную реакцию , а при повышенном содержании ионов Н+ (рН меньше 7) — кислую реакцию . В идеально чистой дистиллированной воде эти ионы будут уравновешивать друг друга.
кислая среда: >
нейтральная среда: =
щелочная среда: >
Когда концентрации обоих видов ионов в растворе одинаковы, говорят, что раствор имеет нейтральную реакцию. В нейтральной воде показатель рН равен 7.
При растворении в воде различных химических веществ этот баланс изменяется, что приводит к изменению значения рН. При добавлении к воде кислоты концентрация ионов водорода увеличивается, а концентрация гидроксид-ионов соответственно уменьшается, при добавлении щелочи - наоборот, повышается содержание гидроксид-ионов, а концентрация ионов водорода падает.
рН показатель отражает степень кислотности или щелочности среды, в то время как «кислотность» и «щелочность» характеризуют количественное содержание в воде веществ, способных нейтрализовывать соответственно щелочи и кислоты. В качестве аналогии можно привести пример с температурой, которая характеризует степень нагрева вещества, но не количество тепла. Опустив руку в воду, мы можем сказать какая вода — прохладная или теплая, но при этом не сможем определить сколько в ней тепла (т.е. условно говоря, как долго эта вода будет остывать).
pH считается одним из важнейших показателей качества питьевой воды. Он показывает кислотно-щелочное равновесие и влияет на то, как будут протекать химические и биологические процессы. В зависимости от величины pH может изменяться скорость протекания химических реакций, степень коррозионной агрессивности воды, токсичность загрязняющих веществ и т.д. От кислотно-щелочного равновесия среды нашего организма напрямую зависит наше самочувствие, настроение и здоровье.
Современный человек живет в загрязненной окружающей среде. Многие приобретают и употребляют пищу, изготовленную из полуфабрикатов. Кроме этого практически каждый человек ежедневно подвергается стрессовому воздействию. Все это оказывает влияние на кислотно-щелочное равновесие среды организма, смещая его в сторону кислот. Чай, кофе, пиво, газированные напитки снижают показатель pH в организме.
Считается, что кислая среда является одной из основных причин разрушения клеток и повреждения тканей, развития заболеваний и процессов старения, росту болезнетворных организмов. В кислой среде до клеток не доходит строительный материал, разрушается мембрана.
Внешне о состоянии кислотно-щелочного равновесия крови человека можно судить по цвету его конъюнктивы в уголках глаз. При оптимальном кислотно-щелочном балансе цвет конъюнктивы ярко-розовый, если же у человека повышается щелочность крови, конъюнктива приобретает темно-розовый окрас, а при повышении кислотности окрас конъюнктивы становится бледно-розовым. При чем цвет конъюнктивы изменяется уже через 80 секунд после употребления веществ, влияющих на кислотно-щелочное равновесие.
Организм регулирует рН внутренних жидкостей, поддерживая значения на определенном уровне. Кислотно-щелочной баланс организма — это определенное соотношение кислот и щелочей, способствующее его нормальному функционированию. Кислотно-щелочной баланс зависит от сохранения относительно постоянных пропорций между межклеточными и внутриклеточными водами в тканях организма. Если кислотно-щелочное равновесие жидкостей в организме не будет поддерживаться постоянно, нормальное функционирование и сохранение жизни окажутся невозможными. Поэтому важно контролировать то, что вы потребляете.

Кислотно-щелочной баланс – это наш индикатор здоровья. Чем мы «кислее», тем скорее стареем и больше болеем. Для нормальной работы всех внутренних органов уровень рН в организме должен быть щелочным, в интервале от 7 до 9.
pH внутри нашего тела не всегда одинаков - некоторые его части более щелочные, а некоторые кислотные. Организм регулирует и поддерживает гомеостаз уровня pH лишь в отдельных случаях, например pH крови. На уровень pH почек и других органов, кислотно-щелочное равновесие которых не регулируются организмом, влияют пища и напитки, которые мы употребляем.
pH крови
Уровень pH крови поддерживается организмом в диапазоне 7.35-7.45. Нормальным показателем pH крови человека считается 7,4-7,45. Даже незначительное отклонение этого показателя влияет на способность крови переносить кислород. Если pH крови повышается до 7,5, она переносит на 75% кислорода больше. При снижении показателя pH крови до 7,3 человеку уже сложно подняться с постели. При 7,29 он может впасть в кому, если показатель pH крови снизится ниже 7,1 — человек умирает.
Уровень pH крови должен поддерживаться в здоровом диапазоне, поэтому организм использует органы и ткани для поддержания его постоянства. Вследствие этого, уровень pH крови не меняется из-за употребления щелочной или кислотной воды, но ткани и органы тела, используемые для регулировки pH крови, меняют свой pH.
pH почек
На параметр pH почек оказывает влияние вода, пища, метаболические процессы в организме. Кислотная еда (например мясные продукты, молочные продукты и др.) и напитки (сладкие газированные напитки, алкогольные напитки, кофе и пр.) приводят к низкому уровню pH в почках, потому что организм выводит излишнюю кислотность через мочу. Чем ниже уровень pH мочи, тем тяжелее приходится работать почкам. Поэтому кислотная нагрузка, приходящаяся от такой еды и напитков на почки, называется потенциальной кислотно-почечной нагрузкой.
Употребление щелочной воды приносит почкам пользу - происходит повышение уровня pH мочи, снижается кислотная нагрузка на организм. Увеличение pH мочи повышает pH организма в целом и избавляет почки от кислотных токсинов.
pH желудка
В пустом желудке содержится не больше чайной ложки желудочной кислоты, выработанной в последний прием пищи. Желудок производит кислоту по мере необходимости при употреблении пищи. Желудок не выделяет кислоту, когда человек пьет воду.
Очень полезно - пить воду на пустой желудок. Показатель pH увеличивается при этом до уровня 5-6. Увеличенный pH будет иметь мягкий антацидный эффект и приведет к увеличению количества полезных пробиотиков (благотворных бактерий). Увеличение pH желудка повышает pH организма, что ведет к здоровому пищеварению и освобождает от симптомов расстройства желудка.
pH подкожного жира
Жировые ткани организма имеют кислотный pH, поскольку в них откладываются излишние кислоты. Организму приходится хранить кислоту в жировых тканях, когда она не может быть выведена или нейтрализована иными способами. Поэтому смещение pH организма в кислую сторону - это один из факторов лишнего веса.
Позитивное влияние щелочной воды на массу тела состоит в том, что щелочная вода помогает выводить из тканей излишнюю кислоту, поскольку помогает почкам работать более рационально. Это помогает контролировать вес, поскольку многократно снижается количество кислоты, которое тело должно «хранить». Щелочная вода также улучшает результаты здоровой диеты и упражнений, помогая организму справиться с излишней кислотностью, выделяемой жировыми тканями в процессе потери веса.
Кости
У костей щелочной pH, так как они в основном состоят из кальция. Их pH постоянен, но если кровь нуждается в регулировке pH, кальций забирается из костей.
Польза, приносимая щелочной водой костям, состоит в их защите, путем снижения количества кислоты, с которым организму приходится бороться. Исследования показали, что употребление щелочной воды снижает рассасывание костей - остеопороз.
pH печени
У печени слабощелочной pH, на уровень которого влияет и пища, и напитки. Сахар и алкоголь должны быть расщеплены в печени, а это приводит к излишкам кислоты.
Польза, приносимая щелочной водой печени, состоит в наличии в такой воде антиоксидантов; установлено, что щелочная вода усиливает работу двух антиоксидантов, находящихся в печени, способствующих более эффективному очищению крови.
pH организма и щелочная вода
Щелочная вода позволяет частям тела, сохраняющим pH крови, работать с большей производительностью. Повышение уровня pH в частях тела, отвечающих за поддержание pH крови, поможет этим органам оставаться здоровыми и работать оперативно.
Между приемами пищи Вы можете помочь Вашему организму нормализовать показатель pH, употребляя щелочную воду. Даже небольшое увеличение pH может оказать огромное влияние на состояние здоровья.
По данным исследований японских ученых, показатель pH питьевой воды, находящийся в диапазоне 7-8, повышает продолжительность жизни населения на 20-30%.
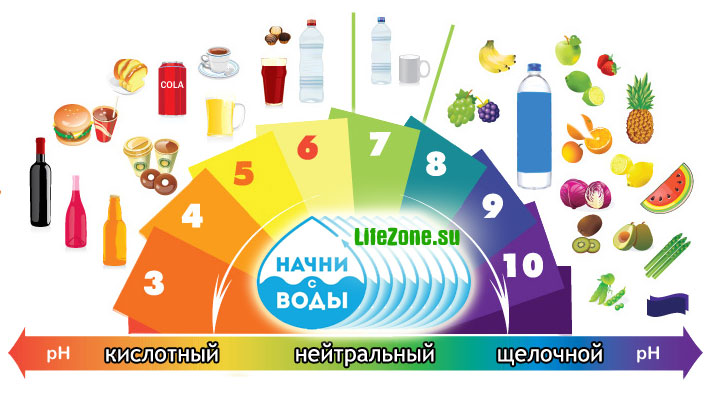
В зависимости от уровня рН воды можно условно разделить на несколько групп:
Сильнокислые воды < 3
кислые воды 3 — 5
слабокислые воды 5 — 6.5
нейтральные воды 6.5 — 7.5
слабощелочные воды 7.5 — 8.5
щелочные воды 8.5 — 9.5
сильнощелочные воды > 9.5
Обычно уровень рН питьевой водопроводной воды находится в пределах, при которых он непосредственно не влияет на потребительские качества воды. В речных водах pH обычно находится в пределах 6.5-8.5, в атмосферных осадках 4.6-6.1, в болотах 5.5-6.0, в морских водах 7.9-8.3.
ВОЗ не предлагает какой-либо рекомендуемой по медицинским показателям величины для рН. Известно, что при низком рН вода обладает высокой коррозионной активностью, а при высоких уровнях (рН>11) вода приобретает характерную мылкость, неприятный запах, способна вызывать раздражение глаз и кожи. Именно поэтому для питьевой и хозяйственно-бытовой воды оптимальным считается уровень рН в диапазоне от 6 до 9.
|
|||||||||||||||||||||||||||||||||||||||||||||||



Интересно знать: Немецкий биохимик ОТТО ВАРБУРГ, удостоенный в 1931 Нобелевской премии по физиологии и медицине доказал, что недостаток кислорода (кислая среда pH<7.0) в тканях приводит к изменению нормальных клеток в злокачественные.
Ученый обнаружил, что раковые клетки теряют способность к развитию в среде, насыщенной свободным кислородом с показателем pH=7,5 и выше! Это означает, что когда жидкости в организме становятся кислыми, стимулируется развитие рака.
Его последователи в 60-х годах прошлого столетия доказали, что любая патогенная флора теряет способность размножаться при pH=7,5 и выше, и наша иммунная система легко справляется с любыми агрессорами!
Для сохранения и поддержания здоровья нам необходима правильная щелочная вода (рН=7.5 и выше). Это позволит лучше сохранять кислотно-щелочное равновесие жидкостей организма, так как основные жизненные среды имеют слабощелочную реакцию.
Уже при нейтральной биологической среде организм может обладать удивительной способностью к самоисцелению.

Не знаете где можно взять правильную воду ? Я подскажу!

Обратите внимание:
Нажатие на кнопку «Узнать » не ведет к каким-либо финансовым тратам и обязательствам.
Вы лишь получите информацию о доступности правильной воды в Вашем регионе ,
а так же получите уникальную возможность бесплатно стать членом клуба здоровых людей
и получить скидку 20% на все предложения + накопительный бонус.

Вступи в международный клуб здоровья Coral Club , получи БЕСПЛАТНО дисконтную карту, возможность участия в акциях, накопительный бонус и другие привилегии!

Водоро́дный показа́тель, pH (произносится «пэ аш», английское произношение англ. pH - piː"eɪtʃ, «пи эйч») - мера активности (в очень разбавленных растворах она эквивалентна концентрации) ионов водорода в растворе, и количественно выражающая его кислотность, вычисляется как отрицательный (взятый с обратным знаком) десятичный логарифм активности водородных ионов, выраженной в молях на один литр: История Это понятие было введено в 1909 году датским химиком Сёренсеном. Показатель называется pH, по первым буквам латинских слов potentia hydrogeni - сила водорода, или pondus hydrogeni - вес водорода. Вообще в химии сочетанием pX принято обозначать величину, равную −lg X, а буква H в данном случае обозначает концентрацию ионов водорода (H +), или, точнее, термодинамическую активность гидроксоний-ионов. Уравнения, связывающие pH и pOH Вывод значения pH В чистой воде при 25 °C концентрации ионов водорода () и гидроксид-ионов () одинаковы и составляют 10 −7 моль/л, это напрямую следует из определения ионного произведения воды, которое равно · и составляет 10 −14 моль²/л² (при 25 °C). Когда концентрации обоих видов ионов в растворе одинаковы, говорят, что раствор имеет нейтральную реакцию. При добавлении к воде кислоты концентрация ионов водорода увеличивается, а концентрация гидроксид-ионов соответственно уменьшается, при добавлении основания - наоборот, повышается содержание гидроксид-ионов, а концентрация ионов водорода падает. Когда > говорят, что раствор является кислым, а при > - щелочным. Для удобства представления, чтобы избавиться от отрицательного показателя степени, вместо концентраций ионов водорода пользуются их десятичным логарифмом, взятым с обратным знаком, который собственно и является водородным показателем - pH. pOH Несколько меньшее распространение получила обратная pH величина - показатель основности раствора, pOH, равная отрицательному десятичному логарифму концентрации в растворе ионов OH − : как в любом водном растворе при 25 °C , очевидно, что при этой температуре: Значения pH в растворах различной кислотности
- Вопреки распространённому мнению, pH может изменяться не только в интервале от 0 до 14, а может и выходить за эти пределы. Например, при концентрации ионов водорода = 10 −15 моль /л, pH = 15, при концентрации ионов гидроксида 10 моль /л pOH = −1.
|
- Для грубой оценки концентрации водородных ионов широко используются кислотно-основные индикаторы - органические вещества-красители, цвет которых зависит от pH среды. К наиболее известным индикаторам принадлежат лакмус, фенолфталеин, метиловый оранжевый (метилоранж) и другие. Индикаторы способны существовать в двух по-разному окрашенных формах - либо в кислотной, либо в основной. Изменение цвета каждого индикатора происходит в своём интервале кислотности, обычно составляющем 1–2 единицы.
- Для расширения рабочего интервала измерения pH используют так называемый универсальный индикатор, представляющий собой смесь из нескольких индикаторов. Универсальный индикатор последовательно меняет цвет с красного через жёлтый, зелёный, синий до фиолетового при переходе из кислой области в щелочную. Определения pH индикаторным методом затруднено для мутных или окрашенных растворов.
- Использование специального прибора - pH-метра - позволяет измерять pH в более широком диапазоне и более точно (до 0,01 единицы pH), чем с помощью индикаторов. Ионометрический метод определения pH основывается на измерении милливольтметром-ионометром ЭДС гальванической цепи, включающей специальный стеклянный электрод, потенциал которого зависит от концентрации ионов H + в окружающем растворе. Способ отличается удобством и высокой точностью, особенно после калибровки индикаторного электрода в избранном диапазоне рН, позволяет измерять pH непрозрачных и цветных растворов и потому широко используется.
- Аналитический объёмный метод - кислотно-основное титрование - также даёт точные результаты определения кислотности растворов. Раствор известной концентрации (титрант) по каплям добавляется к исследуемому раствору. При их смешивании протекает химическая реакции. Точка эквивалентности - момент, когда титранта точно хватает, чтобы полностью завершить реакцию, - фиксируется с помощью индикатора. Далее, зная концентрацию и объём добавленного раствора титранта, вычисляется кислотность раствора.
- Влияние температуры на значения pH
Степень кислотно-щелочных показателей, определяющихся концентрацией водородных ионов, формирует параметры pH, которые в норме для питьевой воды, согласно правилам СанПинН, составляют 6-9 единиц. По этому показателю российские нормативы почти не отличаются от ЕС-директивы - 6,50-9,50 и от требований Агентства США по охране среды (USEPA) - 6,50-8,50.
При этом нормы рН воды, предназначенной для разных отраслевых нужд, отличаются от pH-нормы воды для питья. Например:
- в гидропонике используют растворы с уровнем 5,50-7,50 и разделением этого диапазона на более узкие сегменты в зависимости от конкретного вида растения,
- в общественных бассейнах этот норматив – 7,20-7,40; в частных шире – 7,20-7,60; по DIN 19643-1 – 6,50-7,60,
- при производстве пива используется водная основа с показателями 6,00-6,50,
- для безалкогольных напитков – 3,00-6,00,
- для экспортной водки показатель зависит от жёсткости технологической воды – и равен 7 при жёсткости от 0 до 0,60 мг-экв/л и 6,50 – при 0,61-1,2 мг-экв/л; в водках «внутреннего рынка» – pH <7,80,
- в химическо-волоконном производстве – 7,00-8,00,
- в красильно-отделочном – 6,50-8,50,
- в системах теплоснабжения параметр указывается при температуре +25ºС и находится в пределах 7,00-8,50 для открытых систем и в пределах 7,00-11,00 – для закрытых,
- в энерготехнических и паровых котлах – не меньше 8,50,
- в системах охлаждения: для оборотных и добавочных вод – 6,50-8,50, в циркуляционных холодного контура – 6,50-8,20, горячего контура – 6,80-8,00 и т. д.
Определение уровня и зависимостей pH
Шкала для определения характера кислотно-щелочной среды состоит из 14 единиц, где срединная величина pH=7 считается нейтральной. При смещении по этой шкале к началу (к нулю) растворы приобретают характер кислотных. При смещении к концу – характер щелочных. Чаще всего подобную зависимость отражают в таблицах с частой градацией:

Для сравнения – согласно ГОСТ 6709-96, дистиллят по рН может иметь значения в пределах 5,40-6,60.
Поскольку концентрация ионов водорода низкая (для нейтральной среды – это семь нулей после запятой), то показатель выражается в более привычном виде отрицательным десятичным логарифмом. В таблицах в качестве единиц измерения обычно записывают «pH, ед.» или мкг/л (микрограмм на литр).
Показатель рН отличается от показателя общей щелочности (water alkalinity), которая, выражаясь в мг-экв/л, определяется суммой гидроксильных ионов/ анионов слабых кислот в воде. Низкая щелочность провоцирует резкую смену рН под воздействием внешних факторов.
В природных водах pH, в большинстве случаев, находится в диапазоне 6,50-8,50,отражая зависимость от соотношений с одной стороны – свободного диоксида углерода, с другой – бикарбонат-иона. В болотных водах pH-значения ниже и смещаются в сторону кислотности. Часто именно этот параметр становится индикатором загрязнения на открытых водоемах, демонстрируя наличие стоков с повышенным содержанием кислоты или щёлочи.
При интенсивном фотосинтезе, который наблюдается летом, уровень показателя может повышаться до 8,50-9,00 ед. Также на значения параметра влияет концентрации карбонатов, подверженных гидролизу солей, гидроокисей, гуминовых веществ и др.
Значение уровня pH в повседневной жизни
Японские учёные провели сравнительные исследования потребителей в районах, где пользуются питьевой водой со значениями pH, смещёнными либо в сторону кислотности, либо в сторону щёлочности. Они пришли к выводу, что в районах, где этот показатель выше среднего, люди живут на 20-30% дольше по сравнению со средней продолжительностью жизни по стране. В качестве предположительной причины называется большая «комфортность» кислотных вод для развития патологический микрофлоры.
В связи с тем, что водопроводная вода действительно значительно влияет на состояние здоровья человека, некоторые технические аксессуары, которые контактируют с ней, начинают рекламироваться в качестве средств, способных изменить химические свойства воды. Например, экономители http://water-save.com/ описываются как устройства, которые «обогащают воду слабыми ионами, активизирующими обмен веществ». На самом деле достоверно подтверждается только экономический, но не «целебный» эффект установки экономителя.
Это, однако, не отрицает значения рН-параметра для организма. В каждой среде – в том числе, в различных средах человеческого организма – существуют свои «pH-ориентиры»:
- слюна – 6,8-7,4 (при высокой скорости слюноотделения – 7,8),
- слёзы – 7,3-7,5,
- кровь – 7,43,
- лимфа – 7,5,
- моча – 5,5 (диапазон 5,0-7,5) и т.д.

Для наглядной демонстрации кислотно-щелочного состояния различных сред существуют таблицы, в которых значения расположены в порядке возрастания:



